说明
- 名称解释(7×2)
- 单选(10×2)
- 填空(15*×1)
- 判断(10×1)
- 简答(4个,共22)
- 论述(2个,共19)
0 绪论
- 药物(Medecine):用于预防、治疗或诊断疾病或调节机体生理功能、促进机体康复保健的物质,有4大类:预防药、治疗药、诊断药和康复保健药
化学药物:应用最普遍、数量最多的一类药物
中草药:有几千年的应用历史
生物药物
放射性药物:癌症放射性治疗药物和诊断试剂
-
药品(Drug):药品是指用于预防、治疗、诊断人的疾病,有目的地调节人的生理机能并规定有适应症或者功能主治、用法和用量的物质。 直接用于临床的药物产品,是特殊的商品
-
我国的三大药源:化学药、生物药、中草药
-
中国药典年版分为1部、2部和3部:
药典1部收载药材及饮片,植物油脂和提取物、成方制剂
和单方制剂等;
药典2部收载化学药品、抗生素、生化药品、放射性药品
及药物辅料等;
药典3部收载生物制品,首次将《生物制品规程》并入药典 -
生物药物(Biopharmaceuticals):指运用生物学、医学、生物化学等的研究成果,利用生物体、生物组织、体液或其代谢产物(初级代谢产物和次级代谢产物),综合应用化学、生物技术、分离纯化工程和药学等
学科的重要原理与方法加工、制成的一类用于预防、治疗和诊断疾病的物质。
广义的生物药物包括:
1.从动植物和微生物中制取的各种天然生物活性物质。
2.人工合成或半合成的天然物质类似物。
-
现代生物药物分为四大类:
天然生物药物:1、微生物药物(抗生素) 2、生化药物(含海洋药物)
合成或半合成生物药物
重组DNA药物(又称基因工程或蛋白质药物)
基因药物:以遗传物质DNA、RNA为基础制造的药物
一般把采用DNA重组技术或单克隆抗体技术或其他生物技术制造的蛋白质、抗体或核酸类药物统称为生物技术药物,在我国又称为生物制品
-
抗生素是来源于微生物,利用发酵工程生产的一类主要用于治疗感染性疾病的药物。
-
生化药物是从生物体分离纯化所得到的一类结构上十分接近于人体内的正常生理活性物质,具有调节人体生理功能,达到预防和治疗疾病的物质。
-
生物制品是直接使用病源生物体及其代谢产物或以基因工程、细胞工程等技术制成的,主要用于人类感染性疾病的预防、诊断和治疗的制品。
-
生物制药的定义?
生物制药是利用生物体或生物过程在人为设定的条件下生产各种生物药物的技术,研究的主要内容包括:
各种生物药物的原料来源及其生物学特性
各种活性物质的结构与性质、结构与疗效间的相互作用
生物药物的制备原理、生产工艺及其质量控制等
-
人血白蛋白一直有“生命制品”、“救命药”之称。人血白蛋白是从健康人的血液中提取的,可直接静脉注射到病人体内,主要用于失血创伤、烧伤引起的休克,脑水肿及损伤引起的颅压升高,肝硬化及肾病引起的水肿或腹水,癌症术后恢复等方面的治疗,是临床急救的一种特殊药品。
-
生物碱,是生物体中一类含氮有机化合物的总称,它们有类似碱的性质,能和酸结合成盐。如麻
黄碱、吗啡。 -
强心甙(dai),是一类对心肌有兴奋作用,具有强心生理活性的成分,它们的分子中都
有一个C17位被不饱和内酯环所取代的甾体母核。如洋地黄毒甙 -
.黄酮, 黄酮具有多种药理作用,其中包括:抗氧化作用、消炎作用、抗癌和抗基因诱变作用。
-
皂甙:是一类比较复杂的化合物,它们的水溶液振摇时能产生大量持久的蜂窝状泡沫,与肥皂相似,故名皂甙。它们有减低液体表面张力的作用,可以乳化油脂,用做去垢剂。人参中含皂甙总量约4%。
-
挥发油,是具香味和挥发性、可随水蒸气蒸馏的易流动的油状液体。它们多数具有多方面的药理作用,如解表、发汗、驱风、镇痛、杀虫、抗菌。薄荷、茴香、樟木、桂皮都含有挥发油。
-
树脂,常与挥发油、树胶、有机酸等混合存在,与挥发油共存的称油树脂,与树胶共存的称胶树脂,与芳香族有酸共存的称香树脂。药用的如松香、乳香、没药、安息香等
-
鞣(rou)质,又称丹宁,鞣酸,是存在于植物中的一类分子较大的复杂多元酚类化合物,可与蛋白质结合成不溶于水的沉淀,故能与生兽皮结合而形成致密、柔顺、不易腐败又难以透水的皮革,所以称为鞣质。茶叶、柿子中含有丰富的鞣质。鞣质可用于解毒、抗菌、治疗烧伤(使创面收敛、干燥、结痂)。另外,尚含有氨基酸、蛋白质、酶、激素、糖类、脂类、维生素等生化成分。
-
用埃希氏大肠杆菌生产的天冬酰胺酶是治疗肿瘤的第一个酶制剂。
-
最重要的抗生素产生菌,已有的1000 多种抗生素产自放线菌;还利用放线菌生产氨基酸、核苷酸类、维生素、酶。
-
生物药物定义。
指运用生物学、医学、生物化学等的研究成果,利用生物体、生物组织、体液或其代谢产物(初级代谢产物和次级代谢产物),综合应用化学、生物技术、分离纯化工程和药学等学科的重要原理与方法加工、制成的一类用于预防、治疗和诊断疾病的物质。
-
现代生物药物可分为哪分类。
化学药物、中草药、生物药物、放射性药物
-
生物药物的原料来源。
植物药:高等植物13~15万种,其中药用植物约14500种以上。活性筛选仅占 5%,化学成分研究则更少。我国自然资源丰富,植物品种繁多,其中种子植物就有25700余种,药用植物11800多种,常用5000余种。
动物药 :动物脏器、血液、体液等
海洋生物:海洋占整个地球的表面的71%,蕴藏着极其丰富的生物资源,是展现在人们面前的巨大天然库,现在已成为研究的热点。
微生物:细菌、真菌、放线菌
重组基因工程:基因工程菌、工程细胞、转基因动植物
-
生物药物的特性。
药理学特性,治疗的针对性高、疗效高;营养价值高,毒副作用小;可能具免疫原性或产生过敏反应
原料的生物学特性,原料中有效成分含量低、杂质多;原料的多样性;原料的易腐蚀性
生产制备的特殊性,热、酸、碱、重金属及pH指变化等各种理化因素,甚至机械搅拌剪切力、光照等都会对生物药物活性产生影响。从原料处理、制造工艺过程、制剂、储存、运输和使用环节都要严加控制。
检验的特殊性,理化检验指标;生物活性检验指标;安全性检验指标
剂型要求的特殊性,生物药物易于被人体肠胃道环境变性、酶解,给药途径可直接影响其疗
效的发挥,对剂型大都有特殊要求 -
按药物的化学本质和化学性质,生物药物的分类。
氨基酸类药物及其衍生物
多肽和蛋白质类药物
酶类药物
核酸及其降解物和衍生物
多糖类药物
脂类药物
维生素和辅酶
1 生物药物的质量管理与控制
-
生物药物检验工作的基本程序一般为:
取样,原则:均匀、合理;科学性;真实性;代表性。原料药用取样探子取样:应全批取样,分部位取样;样品量应至少供1次检验使用;取样需填写记录;取样后应混合作为样品
鉴别试剂,鉴别就是依据生物药物的化学结构和理化性质,采用化学法、物理法及生物学方法进行某些特殊反应,或测试某些专属的物理常数,如UV、IR等来判断并确定生物药物及其制剂的真伪。常用鉴定方法,化学反应法、紫外分光光度法、色谱法、酶法、电泳法
杂质检验, 药物的杂质检查主要针对生产中引入的杂质,按照药品质量标准规定的项目,根据生产药品的原料、制备方法、贮藏容器与贮藏过程可能发生的变化等情况,考虑可能存在的杂质,再根据这些杂质的毒性,经综合考虑进行检查。杂质包含的内容:有毒副作用的物质、本身无毒副作用,但影响药物的稳定性和疗效的物质、本身无毒副作用,也不影响药物的稳定性和疗效,但影响药物的科学管理的物质。
安全性检验,异常毒性试验、无菌检测、热原检查、过敏试验、降压物质检查、药代动力学、毒理学
含量测定,指采用化学分析方法或物理分析方法,测定药品的有效成分的含量是否符合规定的含量标准。可用于判定药物的优劣。
检验报告,要求,完整、真实、清楚
-
药物的ADME
A(absorption):药物在生物体的吸收。
D(distribution):药物在生物体的分布。
M(metabolism):药物在体内的代谢转化。
E(excretion):药物及代谢产物自体内的排除。
-
药物的代谢转化一般分为两类反应:
第一类反应:氧化、还原、水解、水合、脱硫乙酰化、异构化等 药物分子上形成-COOH、-OH、-NH2等
第二类反应(结合反应):葡萄糖醛酸化、硫酸酯化、乙酰化、甲基化、氨基酸结合、脂肪酸结合以及缩合等形成极性更高、水溶性更大的代谢产物 -
药物的质量标准
药品质量标准是国家对药品质量、规格及检验方法所做的技术规定,是药品生产、供应、使用、检验和药政管理部门共同遵循的法定依据。
一级标准:中华人民共和国药典(中国药典)
二级标准:中华人民共和国卫生部药品标准(部颁标准)
三级标准:地方各省、市、自治区的地方药品标准
-
我国现行药品质量标准体系
- 国家标准
- 中国药典: (疗效确切、广泛应用、质量可控)
- 部局标准:临床研究用标准(临床研究) ;暂行标准(试生产);试行标准(正式生产初期);地方标准整理提高后的品种
- 企业标准
- 使用非成熟(非法定)方法
- 标准规格高于法定标准
- 国家标准
-
《中华人民共和国药典》缩写 “ChP”
-
5G
GLP:《药品非临床研究管理规范》GLP是Good Laboratory Practice的简称,即药品安全试验规范。主要内容是在规定试验条件下,进行毒性动物试验的准则:对急性,亚急性,慢性毒性试验,生殖试验,致癌,致畸,致突变以及其它毒性试验等临床前安全试验作出规定,是保证药品安全有效的法规。
GCP:《药品临床试验管理规范》GCP是Good Clinical Practice的简称,即药物临床试验管理规范。药品临床试验是指在任何人体(病人或健康的志愿者)进行的药品系统性研究,以证实或揭示试验用药品的作用及不良反应等。制定GCP的目的:保证临床试验过程规范,结果科学可靠,保证受试者的权益并保障其安全。
GMP:《药品生产质量管理规范》GMP是Good Manufacturing Practice的简称,即药品生产质量管理规范。系在药品生产过程中,运用科学、合理、规范化的条件和方法保证生产优良药品的一整套科学管理方法。GMP的实施,确保了制剂生产、管理的规范性。所有医药工业生产,在投产前,对生产过程必须明确规定,所有必要设备必须经过检验,所有人员必须经过适当培训,要求符合规定的厂房建筑及装备,使用合格原料,采用经过批准的生产方法,而且还必需具有符合条件的仓储及运输设施。GMP的三大要素:1)人为产生的错误减小到最低;2)防止对医药品的污染和低质量医药品的产生;3)保证高质量产品的质量管理体系。
GSP:《药品经营质量管理规范》GSP是Good Supply Practice的简称,即药品经营质量管理规范。
是控制医药商品流通环节所有可能发生质量事故的因素从而防止质量事故发生的一整套管理程序。
1992年10月1日起实施,实施GSP必须确保医药商品在购进、验收、入库、贮存、养护、销售、出库、运输、售后服务等流通过程各环节的质量。GAP:《中药材生产质量管理规范》GAP是 Good Agricultural Practice的简称。即中药材生产质量管理规范。是规范药材生产过程,以保证药材质量稳定、可控的一套科学管理方法。涉及到产出药材的药用植物和动物(暂不包括矿物)及其赖以生存的环境、生态;影响药材质量、产量的各种因素(如种质、生物个体、发育等内在因素,气候、土壤、环境、生物(包括人为干扰)等外在因素;有空间变化,也有时间变化)
-
原材料的质量控制
- 目的基因
- 来源和克隆的过程
- 加工过的基因:code、peptide
- PCR技术:primer、enzyme等
- 表达载体
- 载体的生物学性质和来源
- 载体的结构、遗传特性
- 抗生素抗性标志、酶切图谱
- 宿 主
- 宿主的详细资料、载体整合的状态
- 宿主和载体结合后的稳定遗传性资料
- 表达采用的方法及水平
- 目的基因
-
新药研究和开发的主要过程
确定研究计划、准备化合物、药理筛选、化学试验、临床前Ⅰ期、临床前Ⅱ期、Ⅰ期临床、Ⅱ期临床、Ⅲ期临床、注册申请上市、售后检测
-
原料药的研究
化学结构,新药研究最关键和最基础的资料
-
油水分配系数,指当药物在水相和油相达到平衡时,药物在非水相中的浓度和在水相中的浓度之比。
-
脂溶性:影响药物的吸收,影响药物扩散并透过生物膜
-
水溶性:影响药物的溶解和运输,影响药物在体液中的转运
-
生物活性:某些镇痛药的作用强度与油水分配系数呈相关性
-
药物稳定性评价:确定药物的有效期限
有效期:药品在一定的贮存条件下能保持质量的期限
使用期:某特定品种的药品应按规定条件贮存,并在一定时间内使用,过期需经复检,合格方可继续使用
贮存期:药品在一定的贮存条件下不致变质的期限,过期复检合格,可继续贮存一段时间
-
生物药物质量检验的程序和方法
-
ADME
-
5G
-
生物药物常用的定量分析法
- 酶法、电泳法、理化测定、生物检定
2 抗生素概述
- 抗生素:生物在其生命活动过程中产生的(或并用化学、生物或生物化学方法衍生的),在低微浓度下能选择性地抑制他种生物机能的化学物质。
- 半合成抗生素: 将生物合成法制得的天然代谢产物,再用化学、生物或生化方法进行分子改造,制成的各种衍生物,称为半合成抗生素。
将能抑制肿瘤、原虫等微生物产物也归入抗生素类。
-
抗生素的特点
抗生素是微生物次级代谢产物,对微生物本身的生存影响不大。
不同种微生物能产生同一种抗生素,同一种微生物也能产生结构不同的抗生素。
抗生素属于低相对分子质量的次级代谢产物,相对分子质量一般不超过几千。
低微浓度下能选择性地抑制他种生物机能的化学物质。
-
医疗用抗生素应具备的条件:
难使病原菌产生耐药性
较大的差异毒力,“差异毒力”是指药物对病原菌和宿主组织的毒力差异。在宿主体内,对组织不发生或较小发生损害作用,而对病原菌则有较大的毒害。
最小抑菌浓度要低, 抗生素的抗菌活性用**最小抑菌浓度(MIC)**表示,单位mg/mL。
抗菌谱要广,抗生素对各种微生物的抗菌活性称为抗菌谱。
-
如何做到合理用药
针对性要强,最好选用一种药物;
经验用药应先广谱,菌株明确后选择药物;
剂量要足、疗程要够;
掌握既往用药反应;
选择适宜的给药方法;
按医嘱用药:不能随意增量或减量;
有肝肾功能损坏者用药宜慎重,有肾功能损害时要慎用。 -
根据抗生素的生物来源分类:
放线菌:链霉菌属最多,诺卡菌属较少。碱性化合物多。
真菌:担子菌纲稍多,多为酸性化合物。
细菌:主要来源于多黏杆菌、枯草杆菌、短芽孢杆菌、碱性、对肾有毒。
其它:地衣酸、绿藻素、蒜素、番茄素、小蘖碱等。
-
抗生素计量表示法(单组份)
“单位”是衡量抗生素有效成分的一种尺度:一是指定单位;二是活性质量(普遍)。
0.6mg青霉素钠等于一个青霉素单位。
仅以分子结构中活性部分的质量计算。
参照单组份抗生素中活性质量表示方法,以其中某一活性组分的质量作为该抗生素的活性单位
-
抗生素比有机合成农药喷洒浓度低而疗效高,易被土壤微生物分解,对食品危险性小,不会在人体内积累。
-
凝聚:指在投加的化学物质(铝、铁的盐类)作用下,胶体脱稳并使粒子相互聚集成1mm 大小块状凝聚体的过程。
- 凝聚电解质:Al3(SO4)2,AlCl3, FeCl3, ZnSO4, MgSO4
-
絮凝:指使用絮凝剂(天然的和合成的大分子量聚电解质)将胶体粒子交联成网,形成10mm大小絮凝团的过程。其中絮凝剂主要起架桥作用。
- 絮凝剂:人工合成有机高分子聚合物、天然有机高分子聚合物、无机高分子聚合物
-
杂蛋白的去除方法:沉淀法、变性法、吸附法
-
热原是指在药品中污染有能引起动物及人的体温升高的物质,一般认为热原反应主要是由内毒素引起的。
-
管碟扩散法:在培养基凝固以前与“试验菌种”混合,与待检品接触。经过培养后因抗生素的扩散,在抑菌浓度所能达到之处,细菌不能生长形成透明的抑菌范围,此范围一般都呈圆形,称为抑菌圈。扩散法有几种,其中一种叫管碟扩散法(管碟法),在我国作为抗生素效价的法定检定法。
- 抗生素的定义、来源
- 医疗用抗生素应具备的条件
3 现代生物技术在抗生素工业中的应用
- 供体、受体、载体是重组DNA技术的三大基本元件
-
抗生素(链霉素)生物合成基因的结构特点
①链霉菌抗生素生物合成基因组的一个典型特性是高G-C碱基组成,(G+C)%高达70%以上;且三联体密码子中第3个碱基G、C比例极高
②抗生素生物合成基因大多处于一个基因簇中
③抗生素生物合成基因除定位在染色体上外,有的定位于质粒上 -
如何提高抗生素产量
将产生菌基因随机克隆至原株直接筛选高产菌株
增加和敲除合成途径的关键基因
通过调节基因的作用
增加抗性基因
4 生化药品概论
-
生化药物:从生物体分离、纯化所得的一类结构上十分接近于人体内的正常生理活性物质,具有调节人体生理功能,达到预防和治疗疾病目的的物质。
- 特点:来源于生物体;人体的基本生化成分
-
生化药物的特点
-
原材料复杂:
-
同一种生化物质的原料可来源于不同生物体
-
同一种物质也可由同种生物体不同部位产生
-
同一种生物体或组织可产生结构完全不同的物质及结构相似物质
胰岛素:猪、牛、人;
菘蓝:板蓝根、大青叶;
微生物:抗生素、蛋白质、酶等;
-
-
种类多、含量低
-
种属特性不同
-
活性与空间构象有关
-
制备要求高:高营养、低含量、特殊生物活性等决定
-
-
生化药物材料的选择
来源:来源丰富、尽量不与其他产品争原料、最好能一物多用,综合利用。
杂质:难于分离的杂质会增加工艺的复杂性严重影响收率、质量和经济效益 。
有效成分的含量:
合适的生物品种:催乳素,哺乳动物
合适的组织器官 : (胃蛋白酶,胃)
生物的生长期:胸腺素,幼龄动物
合适的种属:人,猪
合适的生理状态:胰岛素,饭后 -
影响提取的因素
- 温度
- 提取温度 ↑溶解度 ↑
- 温度↑ 物料的粘度↓,有利于分子扩散和机械搅拌 对不耐热的生物活性物质的提取,一般在0~10℃有机溶剂提取一般在较低温度下进行
- 酸碱度:抑制有害酶类的水解破坏作用,防止降解,提高收率
- 中性:避免过酸或过碱及等电点,pH4~9
- 酸性:偏酸性介质(胰岛素等),破坏细胞
- 碱性:碱性系统提取(多糖类等)
- 盐浓度:盐离子作用于生物大分子表面,增加了表面电荷,使之极性增加,水合作用增强,促
使其形成稳定的双电层,此现象为盐溶作用。- 与浓度和离子强度有关,高价酸盐作用>单价酸盐
- 温度
-
残留量计算公式
-
分配系数↑,残留物质↑
-
溶剂↑ ,残留量↓
-
提取次数↑ ,残留量↓
-
提取次数↑, 生产设备负担↑,能耗↑,周期↑ ,劳动生产率↓,产品失活
-
生化药物的特点(见上)
-
传统生化制药的一般工艺过程。
- 生物材料的选取与预处理
- 提取有活性部分
- 有效成分的分离与纯化
- 制剂
5 酶类药物
- 原料选择应注意的问题
- 了解目的酶在生物材料中的分布特点,选择适宜的生物原料。如乙酰化氧化酶在鸽肝中含量高,提取此酶时宜选用鸽肝为原料;凝血酶提取选用牛血;透明质酸酶选用羊睾丸;溶菌酶选用鸡蛋清;超氧化物歧化酶选用血和肝脏等。用微生物生产酶时需根据酶活力测定,来决定提取时间。
- 考虑生物在不同发育阶段及营养状况时,酶含量的差别及杂质干扰的情况。如从鸽肝提取乙酰化酶,在饥饿状态下取材,可排除杂质肝糖原对提取过程的影响;凝乳酶只能用哺乳期的小牛胃作材料等。
- 用动植物组织作原料,应在动物组织宰杀后立即取材。
- 考虑生化制备的综合成本,选材时应注意原料来源应丰富,能综合利用一种资源获得多种产品。还应考虑纯化条件的经济性。
-
药用酶原料选择应注意的问题(见上)
-
简述天冬酰胺酶的生产工艺

图片alt
6 糖类药物
-
糖是机体的组成成分之一,如葡萄糖存在于一切组织中;糖原(又叫动物淀粉)在肝及肌肉中含量最多,如肝糖,约占肝质量的18%;核糖及脱氧核糖是核酸及核蛋白不可缺少的组成成分;细胞间质及结缔组织中含有大量的粘多糖类物质。
-
寡糖不仅以游离状态参与生命过程,而且往往以糖缀合物(**糖蛋白、糖脂)**的形式参与许多重要的生命活动。
-
多糖类的生理功能
调节免疫功能和抗肿瘤作用;
抗感染作用;
促进细胞DNA、蛋白质的合成;
抗幅射损伤作用;
抗凝血作用;
降血脂,降血胆固醇,抗动脉粥样硬化。 -
1.6-二磷酸果糖(FDP)-生产工艺
-
酶转化法:
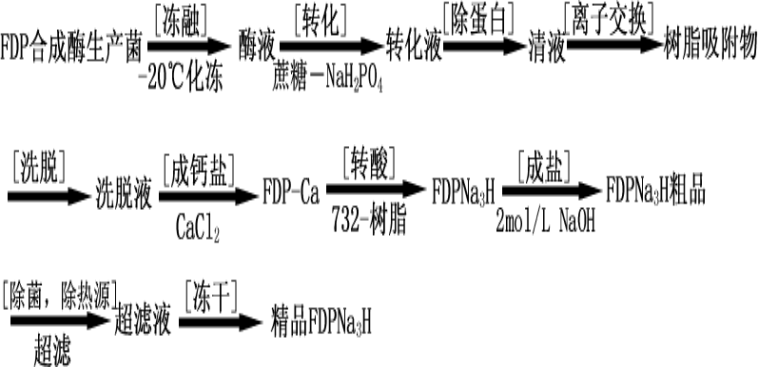
图片alt
- 固定化细胞制备工艺:

图片alt
- FDP的生产工艺(见上)
- 多糖类药物的生理功能
糖的主要生理功能在于供给机体所需的能量,维持人体的日常劳动、工作以及一切生理活动。同时不少糖类物质及其衍生物具有药用价值
低聚糖的生理功能:
1.低热值、防肥胖;
2.抑制腐败菌生长繁殖;
3.增殖作用;
4.抗龋齿、抗肿瘤
多糖类的生理功能:
1.调节免疫功能和抗肿瘤作用;
2.抗感染作用;
3.促进细胞DNA、蛋白质的合成;
4.抗幅射损伤作用;
5.抗凝血作用;
6.降血脂,降血胆固醇,抗动脉粥样硬化。